醫療器械臨床試驗稽查分為項目稽查�����、系統稽查、供應商稽查(比如:CRO公司選擇��、中心實驗室選擇等)�,一般情況下針對臨床試驗機構的項目稽查居多。政策和執法尺度不斷在變化����,項目稽查可以從臨床試驗中機構選擇�、臨床試驗操作到臨床試驗結束貫穿整個臨床試驗的全部過程���,依照現行法規對臨床試驗項目進行全方位的稽查��。
醫療器械臨床試驗稽查分為項目稽查��、系統稽查、供應商稽查(比如:CRO公司選擇、中心實驗室選擇等),一般情況下針對臨床試驗機構的項目稽查居多。政策和執法尺度不斷在變化,項目稽查可以從臨床試驗中機構選擇��、臨床試驗操作到臨床試驗結束貫穿整個臨床試驗的全部過程����,依照現行法規對臨床試驗項目進行全方位的稽查。
醫療器械臨床試驗稽查一般流程如下:
1、企業委托第三方稽查公司��,簽訂稽查協議��。
2�、第三方稽查公司接收臨床試驗項目相關資料����,包括但不限于臨床試驗方案�����、ICF���、CRF��、原始記錄等相關文件。
3����、企業和第三方稽查公司共同確定被稽查的臨床試驗機構和稽查時間��。
4、第三方稽查公司組建稽查團隊���,制訂稽查方案、稽查記錄表格等��。
5��、企業向被稽查的機構提出稽查申請���,發出稽查函�,獲得機構批準����。
6、第三方稽查公司在臨床試驗機構召開稽查啟動會��,向臨床試驗機構的有關人員介紹本次稽查的目的�����、內容和程序���,并請主要研究者介紹臨床試驗的有關情況����。
7��、請求研究者的協助�,請其向相關輔助科室發出稽查通知�,獲得輔助科室的配合。
8�、派遣稽查人員進駐臨床試驗機構進行現場稽查���,對研究者文件夾�、知情同意書�����、原始文件/病例報告表���、機構HIS���、LIS系統等進行稽查�。
9��、根據發現的問題提出建議并分別與研究者����、機構老師確認并溝通解決辦法����。
10、整理稽查記錄及問題�,完成稽查報告�����。
11���、與申辦方溝通���,完成整改報告���。
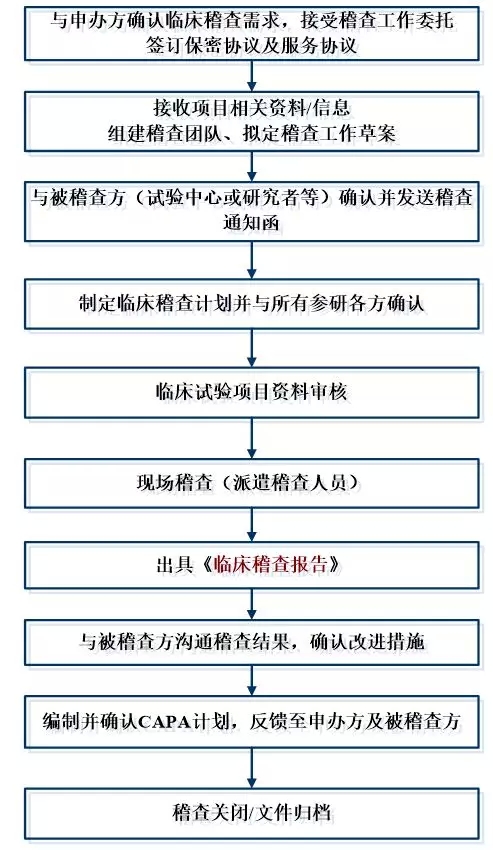
醫療器械臨床試驗稽查流程圖: